理科の動画「化学計算総合①」を見ました。
この単元でも完全中和する時の比や、質量保存の法則から重さを出すときの比、を使います。後半ではつるかめ算を使用した計算も出てきますので、算数の出来も左右しますが、同じようなパターンの問題も多いので、しっかりと得点できる単元にしましょう!

問題をよんで問題の条件をしっかり確認しましょう!
〜基礎編〜
コアプラスの解説
人体の再徹底の確認です。
(7)胎児のへその緒の問題です。胎盤は境目があって、母体と栄養のやり取りをします。胎児から胎盤へは動脈で二酸化炭素や不要物を、胎盤から胎児へは静脈で養分や酸素を渡されます。
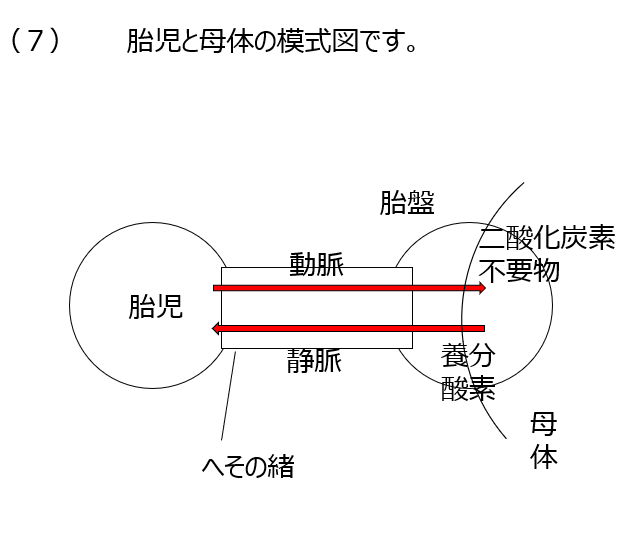
]
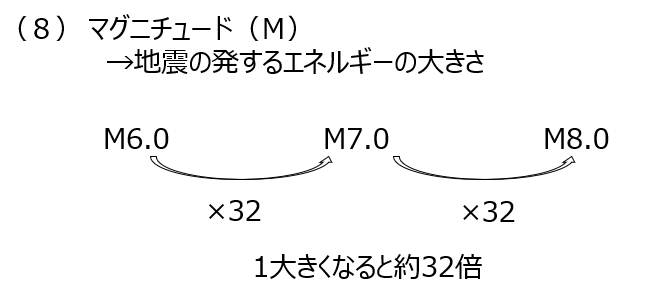
(8)マグニチュードは地震の発するルエネルギーの大きさです。マグニチュードが1大きくなると32倍大きくなります。マグニチュードが2大きくなると、32×32倍、となります。
(9)震度はその地点での「ゆれ」の大きさです。最大震度は7です。0,1,2,3,4,5弱、5強、6弱、6強、7、の10段階です。

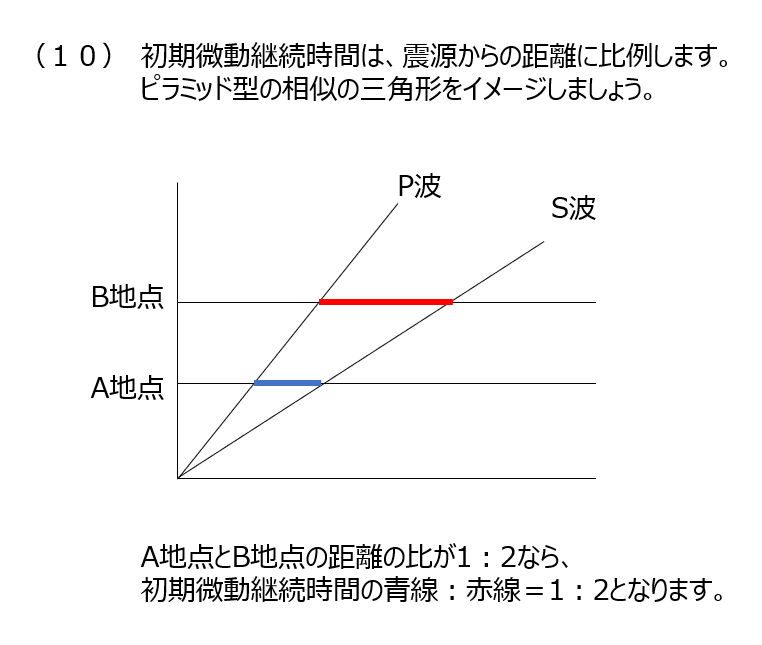
(10)P波とS波があります。P波がすぐに届きます。初期微動継続時間です。P波とS波が届く時間の差が大きければ、震源から遠い、となります。
デイリーチェック
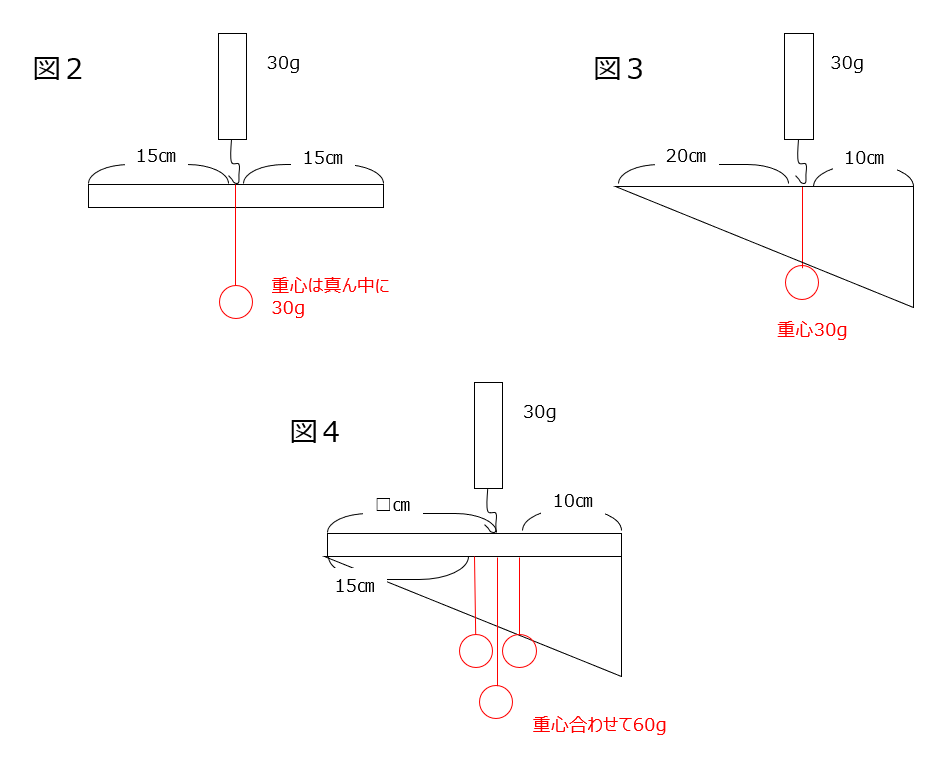
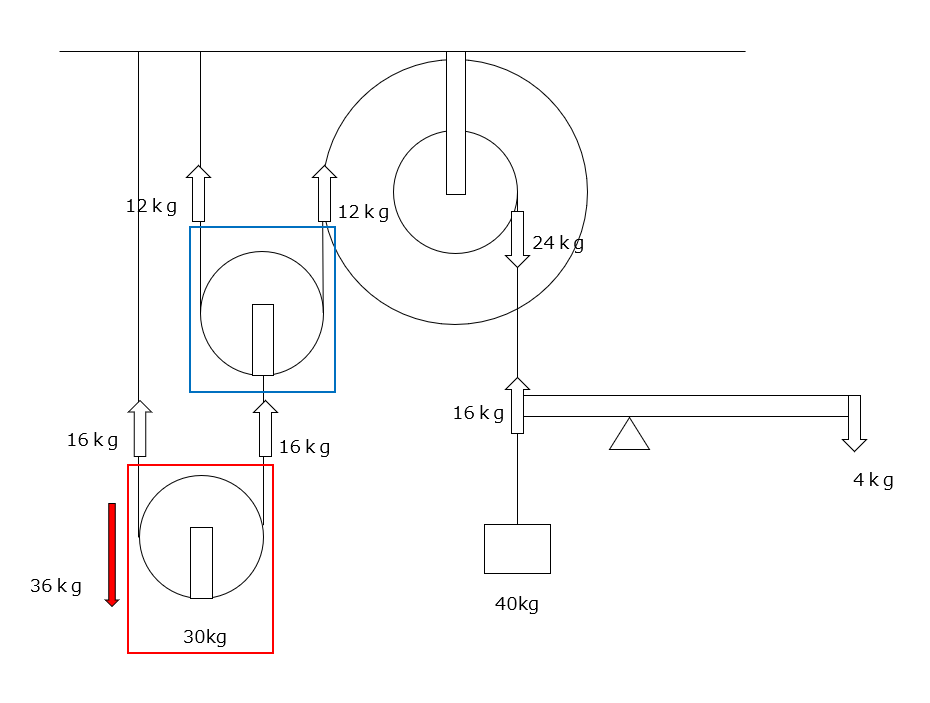
1⃣(2)図2,図3できちんとおもりの重さを書いておいてから、図4を考えるようにしましょう。重心を合わせて考えます。(3)Aから順に考えていきます。
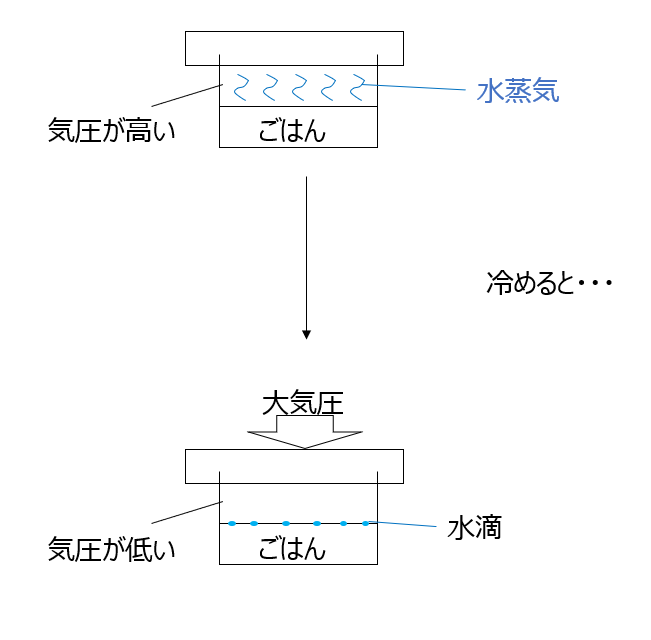
2⃣(1)①勝ち負けをまとめて書いてみましょう。(2)はお弁当の話です。ご飯の水蒸気と水滴の話です。水滴になると、お弁当の中の気圧が低くなります。

確認問題の解説
確認【1】
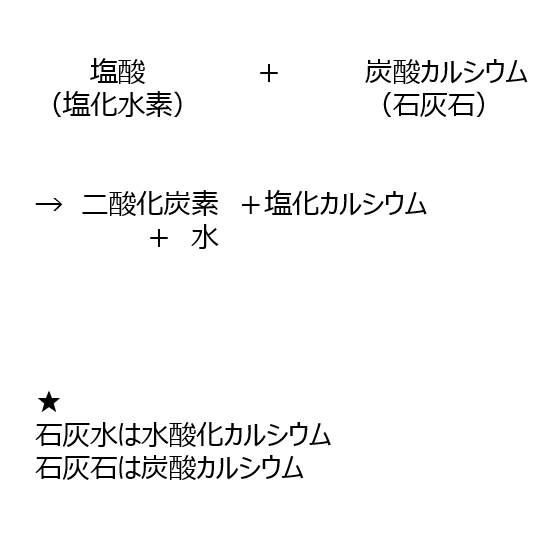
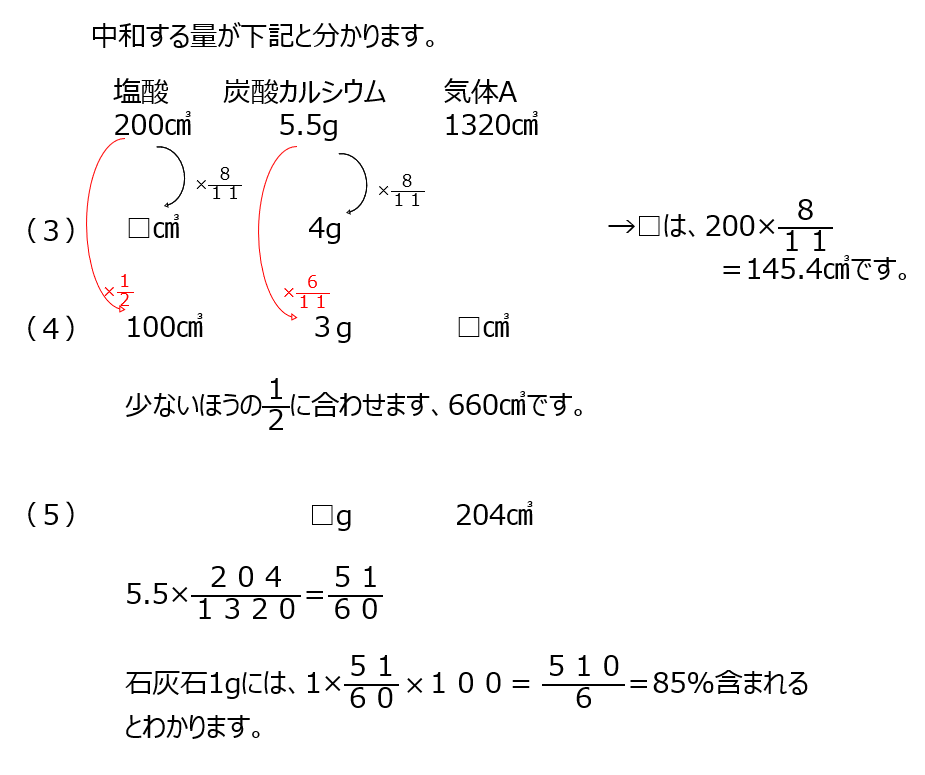
(1)塩酸(塩化水素)と炭酸カルシウム(石灰石)を混ぜると、二酸化炭素と塩化カルシウムと水、ができます。
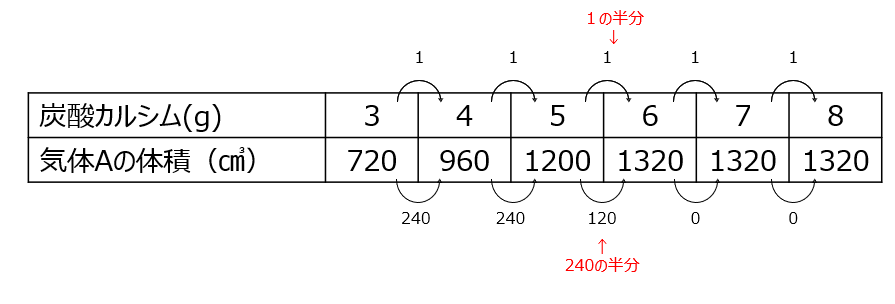
(3)~(5)表の各差を見て、正比例で増加しない部分に注目します。炭酸カルシウムが5.5gの時に完全に中和した、と考えます。少数点第一位を四捨五入しますよ。比を書いて、反応が少ないほうに揃えて考えていく、のは、今までと同じ考え方ですよね。
確認【2】
ガスバーナーの使用手順はしっかり覚えましょう、ガスよりも先にマッチに火を付けますよ。
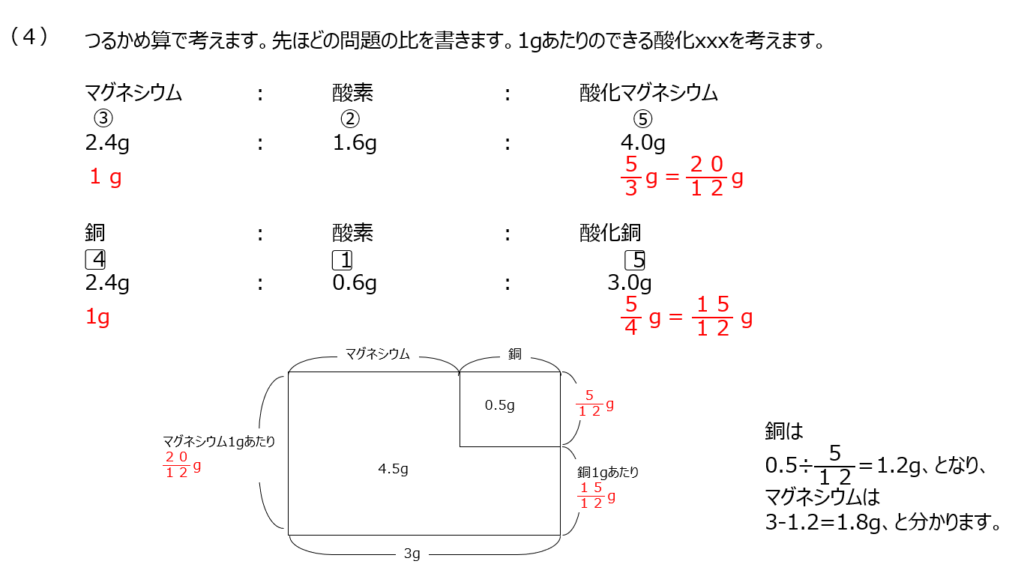
マグネシウムと酸素の反応です。マグネシウムとちょうど反応する酸素と酸化マグネシウム、の比から考えていきます。同じように、銅と酸素と酸化銅の比から考えます。酸化銅の差から反応した酸素の量がわかります。(4)ではつるかめ算になりますので、面積図を書いて求めますよ。わからない場合は動画確認をお勧めします。

確認【3】
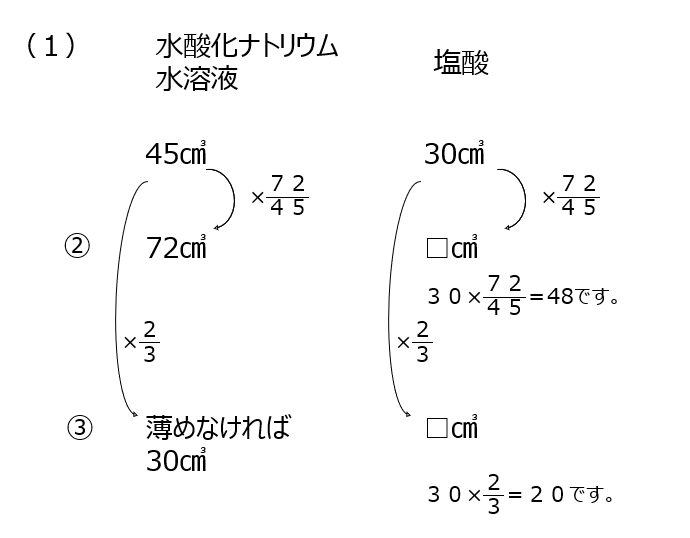
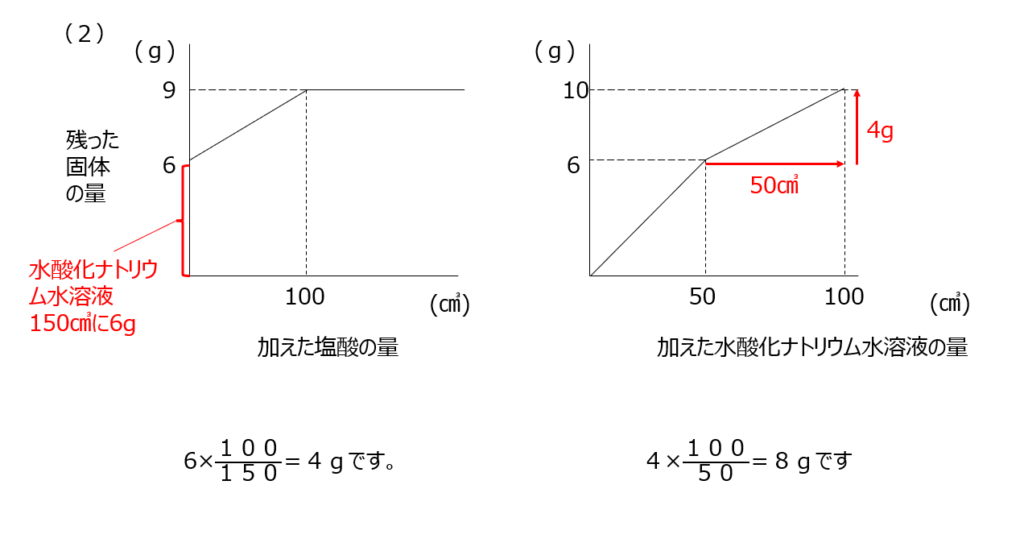
中和計算の問題です。水酸化ナトリウム水溶液と塩酸の中和です。BTB溶液の色はきちんと覚えておきましょうね。完全中和になるときの比を用いて、少ないほうに合わせて考える、今までと同じ考え方になります。グラフを読み解く問題もあります。
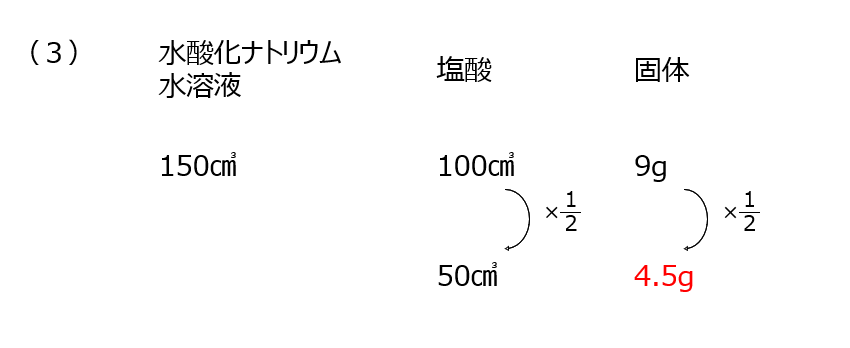
確認【4】
過酸化水素と二酸化マンガンによって酸素と水ができる問題です。二酸化マンガンを増やすと過酸化水素と触れる面積が増えるので、反応時間が早くなります。質量保存の法則、から反応する水の量がわかります。
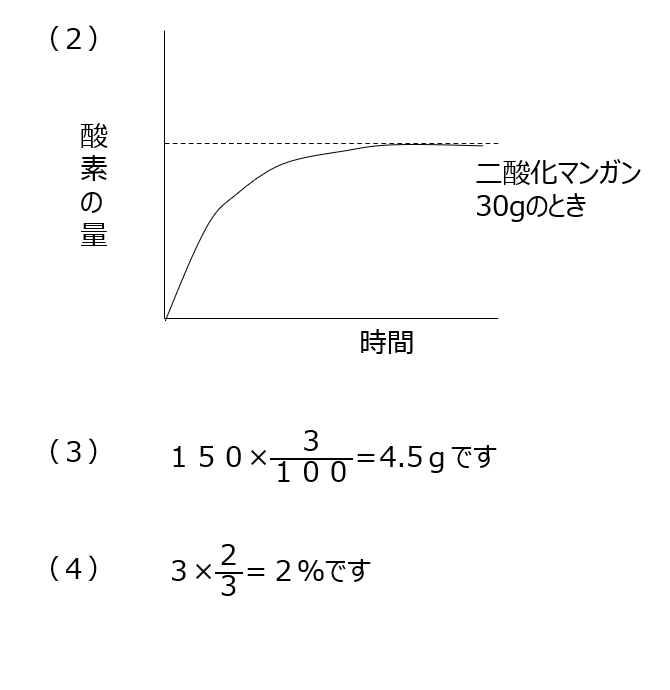
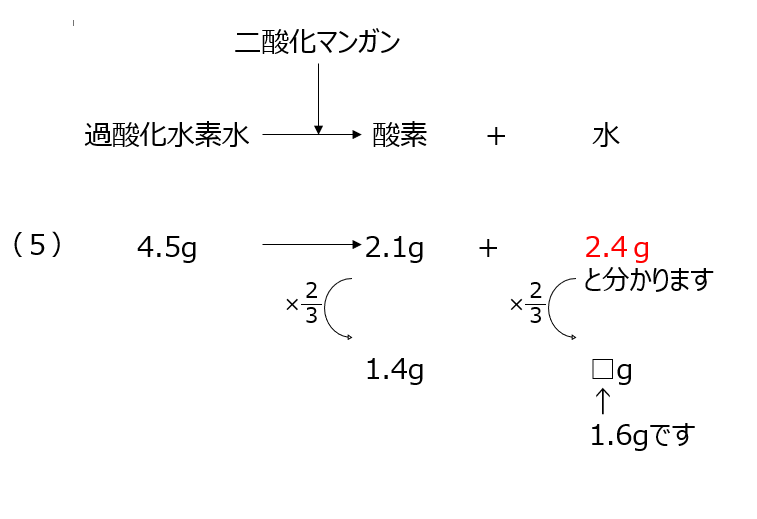
確認【5】
オキシドールと二酸化マンガンの反応問題です。表の値とグラフを考える問題です。濃度や反応時間からグラフの違いを考えます。
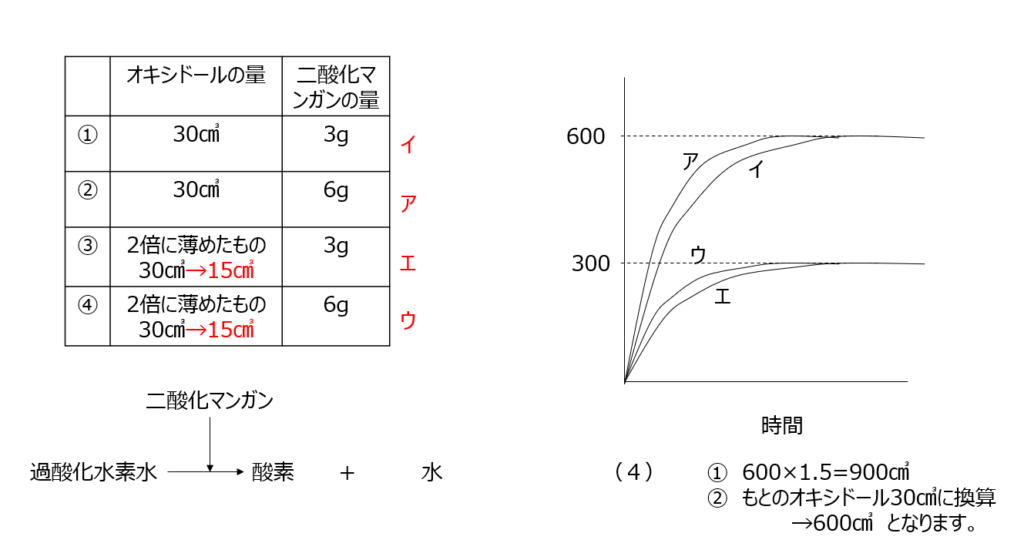
〜標準編〜
確認問題の解説
確認【8】
特殊な実験なので、問題文をしっかり読みましょう。表から差を読み取ります、差は発生した気体の重さです。蓋を緩めなければ重さは変わっていませんので、質量保存の法則、が成り立ちます。塩酸と石灰石が完全反応する量を比例から求めます。
確認【10】
酸化銅を銅に戻す、という問題です、還元の問題です。炭素を増やしていき、反応することで残った個体は減っていきますが、増やしすぎると余ってくるようなグラフを書きます。酸化銅とたんとが反応して、銅と二酸化炭素ができる、という比を求めます。酸化銅は還元されています、炭素は酸化されて二酸化炭素ができます。
確認【12】
塩酸と鉄の反応を2つのグラフを見ながら解きます。塩酸と鉄と発生する気体の比をわかる部分を書き出して合わせて、3つの関係の比を出します、算数の「連比」のような考え方です。(4)ではつるかめ算になりますので、図を書いて解きます。
確認【13】
塩酸とアルミニウムの反応の問題です。塩化アルミニウムと水素ができます、質量保存の法則、も使います。気体が空気中に逃げたので全体の質量が変わっていることに気づきましょう。
〜発展編〜
確認問題の解説
確認【14】
濃さの違う水溶液の中和計算の問題です、濃さをそろえて計算するなどして解き進めます。水酸化ナトリウムを加えていく場合は、中和が終わった後も固体が増えていくので、つるかめ算が必要になるケースが多いです。単位量当たりの固体の増加、を考えます。単位当たりなので計算がややこしいです、分数を約分せずに図に記載して解き進める方法を動画では説明があります。AとCをそろえることで、(4)を解くことができますね。(5)では量や濃さを変えて解き進めます。これも動画ではとても分かりやすく説明有りますよ。
発展問題の解説
発展【1】
表では数値がそろっていない為わかりにくいです。表の値を2倍したり3倍したり、することでどちらかを揃えます。この問題では、塩酸の量を最小公倍数の12で揃えて、反応の量を変えて書き直します。この問題も、水酸化ナトリウムを増やしていく、および、完全中和がわからないので、つるかめ算を使用する方針となります。
まとめ
つるかめ算か何度も出てきましたが、水酸化ナトリウムが余る場合で、中和点が表から読み取れない場合、しかありませんでしたね。ここも苦手意識を持たずに、いつもと同じパターン、と思って得点できるようにしましょう!
最後まで読んで頂きありがとうございました。
下記に他の動画解説のページもありますので、紹介させてください。
参考になるとうれしいです。




コメント